La mise sous silence de ces gènes implique un groupe de protéines appelées Complexes Répressifs Polycombes, ou PRC. Les PRC produisent ce que l'on appelle des changements épigénétiques, qui réduisent l'activité des gènes spécifiques à la lignée qui permettraient à une cellule souche de devenir un type de cellule plus spécialisé.
La redondance est qu'il existe deux groupes distincts de PRC, et que les deux groupes travaillent indépendamment et simultanément pour faire taire les mêmes gènes spécifiques à la lignée. Si le premier groupe de PRC cesse de travailler, le deuxième groupe peut alors s'en charger. Si le groupe 2 échoue, le groupe 1 est une solution de secours.
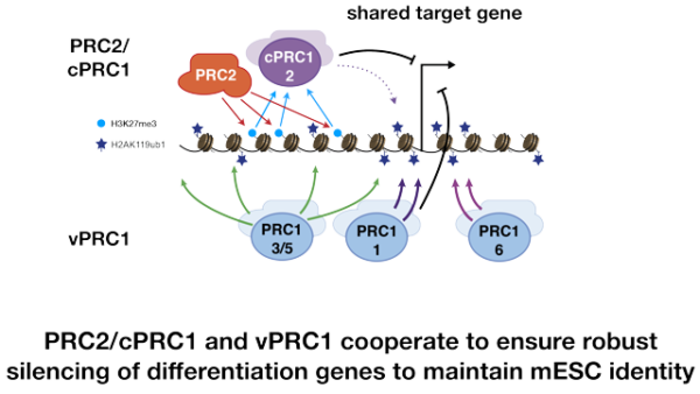
"Nos résultats concilient les observations précédentes selon lesquelles l'une des PRC, à savoir la PRC2, n'est pas nécessaire pour l'auto-renouvellement des cellules souches embryonnaires de souris. Nous montrons maintenant que la PRC2 est essentielle pour diriger l'activité de la cPRC1 afin de maintenir la répression des gènes cibles spécifiques à la lignée, lorsque la fonction de la vPRC1 est compromise", a déclaré M. Bell. "Ainsi, les PRC coordonnent des mécanismes redondants qui assurent une répression robuste des gènes clés de spécification de la lignée, non seulement pour la différenciation, mais aussi pour le maintien de l'identité des cellules souches embryonnaires de souris".
Parmi les autres co-auteurs, on peut citer : Carina Pribitzer, Jingkui Wang, Thomas R. Burkard, Brian Reichholf, Julian Jude, Hagar F. Moussa et Johannes Zuber du BioCenter de Vienne ; Daniel Bsteh du BioCenter de Vienne et de l'USC ; et Silvia Golumbeanu, Qing (Sunny) Zhao et Suhn Kyong Rhie de l'USC.
Cinq pour cent de ces recherches ont été financées au niveau fédéral par une subvention des National Institutes of Health des États-Unis (K01CA229995). Quatre-vingt-quinze pour cent ont été financés par d'autres sources : l'Académie autrichienne des sciences, le groupe New Frontiers de l'Académie autrichienne des sciences (NFG-05), le Human Frontiers Science Programme Career Development Award (CDA00036/2014-C), le USC Norris Comprehensive Cancer Center et une bourse de doctorat du Fonds Boehringer Ingelheim.
Traduction Sott.net - Source : University of Southern California



Commentaires des Lecteurs
Lettre d'Information